徐駿森教授團隊解析中東呼吸症候群冠狀病毒蛋白質有藥物開發潛力
KAIMRC innovations報導臺大徐駿森教授團隊解析中東呼吸症候群冠狀病毒之蛋白質結構有藥物開發潛力,農業化學系/基因體與系統生物學位學程/系統生物學中心徐駿森教授團隊利用結構生物學與生物物理方法,解析在中東呼吸症候群冠狀病毒(MERS-CoV)基因體中會結合磷酸二腺苷核糖(ADP-ribose)的蛋白質模組之三維結構,可望成為發展新藥的潛力標靶。該研究已發表於2016年的「Journal of Biological Chemistry, 生物化學期刊」,並被沙烏地阿拉伯阿布都拉國王國際醫學研究中心(King Abdullah International Medical Research Center, KAIMRC)發行之國際雜誌KAIMRC innovations (Nature Publishing Group)與網站以International Research Highlight採訪報導。
受訪時徐駿森老師表示:「ADP-ribose是細胞中廣泛存在的代謝物,主要是源自磷酸二腺苷核糖基化(ADP-ribosylation)這種後轉譯修飾作用。細胞中存在可以辨識ADP-ribose的蛋白質模組稱為macro domain,細胞中已知含有macro domain的蛋白質參與調控許多重要的細胞生理功能。冠狀病毒基因組中存在具有保守性的macro domain,在相似的病毒中,如SARS-CoV,macro domain是重要的致病因子,其酵素活性與抑制宿主免疫反應有很大的關聯。相較於十多年前爆發的SARS,新興的MERS致死率是SARS的四倍,自從2012年在中東出現病例之後,短短幾年間已造成超過六百人的死亡,而且目前尚無治療方法,因此尋找能夠當作藥物標靶的病毒蛋白質並設計抑制藥物一直是科學家們研究的重點。」
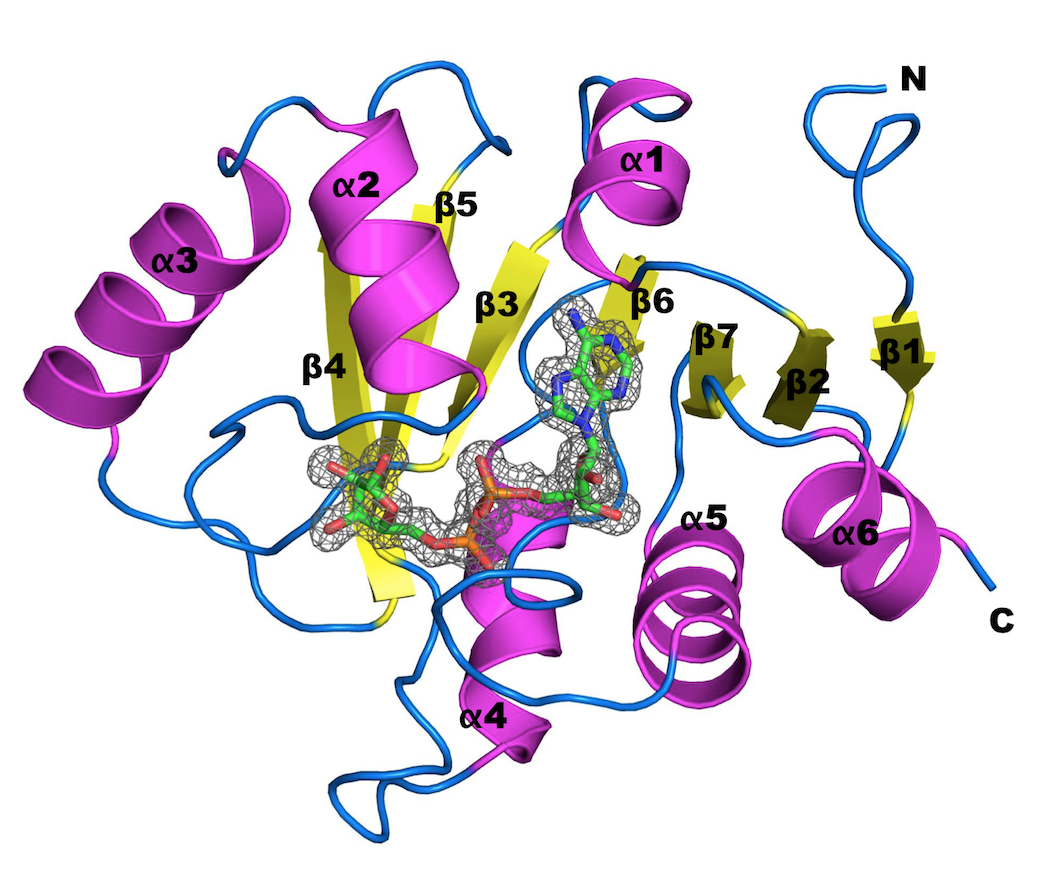
論文第一作者為基因體與系統生物學位學程博士班卓昭成同學,卓同學也以此著作獲得衛生福利部傳染病防治研究及教育中心大專生及研究生優秀著作獎之傑出獎(第一名)。卓同學表示,「利用分子交互作用的生化分析,我們發現MERS-CoV macro domain相較於其他的冠狀病毒的macro domain來說,能夠更…(全文詳網頁)有效率的結合ADP-ribose。我們更進一步得到高解析度的MERS-CoV macro domain與ADP-ribose的複合體結構,並發現造成結合效率改變的原因可能是由於α1螺旋中存在的結構性差異改變了具有保守性的天門冬胺酸與ADP-ribose之間的交互作用。我們研究顯示MERS-CoV有可能利用macro domain去調節細胞中的ADP-ribosylation修飾並影響宿主的免疫反應。」
先前的藥物設計多是針對病毒的刺突蛋白質與人類的受體蛋白質之間的交互作用,但是目前MERS仍然沒有有效的治療方法,發現新的標靶蛋白質有機會能治療這種新興傳染病,而得到該蛋白質的三維結構更能夠加速設計小分子藥物的過程。例如可以利用食品小分子與中草藥資料庫,或是已在使用的西藥資料庫為篩選對象,尋找具有潛力的藥物。
參考資料:1. Chao-Cheng Cho, Meng-Hsuan Lin, Chien-Ying Chuang, Chun-Hua HsuMacro Domain from Middle East Respiratory Syndrome Coronavirus (MERS-CoV) Is an Efficient ADP-ribose Binding Module: CRYSTAL STRUCTURE AND BIOCHEMICAL STUDIES. (2016) J Biol Chem 291(10):4894-4902.
2. https://innovations.kaimrc.med.sa/en/research/26/promising-protein-target